
RNA-LNP terapisi üretimi altı ana adıma ayrılabilir (Şekil 1, sol):
1) Fermentasyon yoluyla pDNA şablonunun üretimi, 2) mRNA ilaç maddesini oluşturmak için in vitro transkripsiyon (IVT) reaksiyonu,
3) mRNA'nın kromatografi ve eğik akış filtrasyonu (TFF) ile saflaştırılması, 4) RNA-LNP ilaç ürününün, RNA'nın lipitlerle etanol içinde karıştırılması ve ardından çevrim içi seyreltilmesi yoluyla oluşumu, 5) Etanolün TFF ve steril filtrasyon yoluyla uzaklaştırılması, 6) Aseptik doldurma ve şişelere son işlem. Adım 4'te RNA'nın bir LNP içinde kapsüllenmesi, yüksek verimlilik oranları ve büyük parti boyutları için ölçeklenmesi en zor bir birim işlemlerden biridir; çünkü bu adım RNA ve lipitlerin yüksek kontrollü bir şekilde karıştırılmasını gerektirir. Karıştırma süreci, ilaç ürününe özgüdür ve ilaç ürününün fiziksel özelliklerini, potansiyelini ve toksisitesini etkiler. Ayrıca, RNA-LNP'ler için tam ölçekli süreç geliştirme yapmak maliyet açısından yasaklayıcı ve zaman alıcıdır.
RNA-LNP ilaç ürünleri geliştikçe ve keşif aşamasından süreç geliştirme ve ticari üretim aşamasına geçtikçe, düzenleyici gerekliliklere uyum giderek daha önemli hale gelir. Geç aşama süreç geliştirmeden ticari üretime geçerken dört düzenleyici gereklilik göz önünde bulundurulmalıdır:%100 etanol genellikle lipitleri çözmek için kullanılır ve yanıcı sıvı olarak sınıflandırılır, bu da etanolün ortam sıcaklıklarında havada tutuşabileceği anlamına gelir. Yerel düzenlemeler, yanıcı bir sıvıyı işlemek için Patlayıcı Ortam (HazLoc) dereceli ekipman gerektirebilir. İki HazLoc sertifikası ATEX (Patlayıcı Atmosferler için Avrupa Belgesi) ve IECEx (Patlayıcı Ortamlar İçin Ekipman Standartlarına İlişkin Uluslararası Elektroteknik Komisyonu Sertifikasyon Sistemi) sertifikalarıdır.Elektronik kayıtları destekleyen yazılım, FDA 21 CFR Part 11 uyarınca düzenlenmiş bir ortamda kullanılmak için uygun olmalıdır.Sistemin biyokütlesi, süreç validasyonunu desteklemek amacıyla kontrol edilmelidir; bu, temizleme ve sonrasında validasyon (CIP) veya gama ışını ile sterilize edilmiş tek kullanımlık teknolojiler (SUT'ler) kullanılarak sağlanabilir.Sıvı temas eden malzemeler, Amerika Birleşik Devletleri Farmakopesi (USP) <665> yönergelerine göre ekstraktabl ve sızdırılabilirlik (E&L) açısından değerlendirilmelidir.Precision NanoSystems, RNA-LNP üretimi için NxGen karıştırma teknolojisini kullanan NanoAssemblr® ekipman serisini geliştirmiştir. Özellikle, sıvı kanalları ilk olarak iki boyutta geliştirilmiştir: NxGen ve NxGen 500. Bu, RNA-LNP'lerin geniş bir akış hızları ve hacimler aralığında yüksek tekrarlanabilirlik ve ölçeklenebilirlik ile üretilmesini sağlar ve toplu yöntemlerin (örneğin, türbülanslı in-line karıştırma) ana sınırlamalarını aşar. Tüm NxGen karıştırma kartuşları tek kullanımlıktır, bu da partiler arasında çapraz kontaminasyon riskini azaltır. NanoAssemblr® Ignite™ ve Ignite+™, preklinik formülasyon geliştirme, optimizasyon, erken süreç geliştirme ve hilti işlem parametreleri üzerinde çalışmak için 1–60 mL RNA-LNP üretir. NanoAssemblr Blaze™ ve Blaze+™, ölçekleme için ve amam üst ve alt süreç geliştirme için 10 L'ye kadar üretim yapabilir.
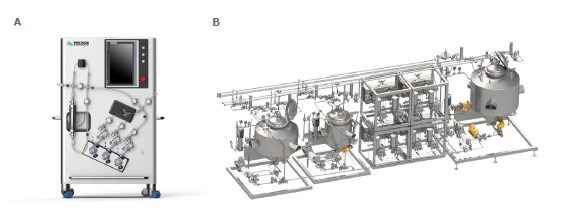
Precision NanoSystems, 21 CFR Part 11 uyumlu yazılım sağlayan, ATEX ve IECEx sertifikalı iki sistem geliştirmiştir ve NxGen ticari kartuş 48 L/saat akış hızına sahip sistemleri klinik ve ticari RNA-LNP üretiminde kullanmaktadır. NanoAssemblr ticari formülasyon sistemi (Şekil 2A), klinik fazlar 1–3 ve ticari üretim için 0,5 ila 400 L arasında değişen parti büyüklüklerinde RNA-LNP üretimi yapmak üzere tasarlanmıştır. Bu sistem, NxGen 500 karıştırıcı (NxGen ticari kartuş 12 L/saat olarak pazarlanan) veya uygun olduğunda NxGen ticari kartuş 48 L/saat kullanılarak ön-dilütasyon sırasında 6 ila 48 L/saat (100 ila 800 mL/dakika) LNP akış hızlarını destekler. Partiler arasında dönüş süresini azaltmak ve farklı iş akışları arasında çapraz kontaminasyonu ortadan kaldırmak için sistem, pompalar, akış metreleri ve bir NxGen kartuşunu içeren gama ışını ile sterilize edilmiş tek kullanımlık bir sıvı yolunu kullanır. Ticari formülasyon sistemi hem NxGen 500 hem de yeni NxGen ticari kartuş 48 L/saat’i destekler. NanoAssemblr modüler ticari formülasyon skid’i (Şekil 2B), faz üç gen düzenleme, protein yerine koyma tedavileri ve pandemik yanıt aşıları gibi uygulamalar için 400 L ile 3200 L arasında büyük ticari üretim partileri üretmek üzere tasarlanmıştır. Bu skid, kullanıcı gereksinimlerine göre yapılandırılabilir ve RNA-LNP'leri saatte 384 L'ye kadar üretmek için aynı anda sekiz NxGen ticari kartuş kullanır.Bu çalışmada, ticari formülasyon sisteminin ve modüler ticari formülasyon skid’inin yeteneklerini ve küçük ölçekli LNP üretiminden büyük ölçekli ticari üretime hızlı geçişi sağlayan ilgili iş akışını gösteriyoruz. İlk olarak, NxGen, NxGen 500 ve NxGen ticari kartuş 48 L/saat kullanılarak üretilen POPClipozomlarının akış hızındaki artışa yanıt olarak tahmin edilen sınır-boyut davranışını takip ettiğini ve 48 L/saat (800 mL/dakika) akış hızlarında yüksek kaliteli lipozomların üretilebileceğini gösteriyoruz. NxGen teknolojisinin ölçeklenebilirliğini göstermek için, mRNA yerine geçebilecek bir plazmid DNA kullanarak NxGen ticari kartuş 48 L/saat ile 50 L'ye kadar pDNA-LNP partileri hazırladık. Son olarak, SARS-CoV-2 için kendi kendini çoğaltan mRNA (saRNA) LNP aşı adayının dağıtımını nasıl basitleştirebileceğini göstermek amacıyla klinik olarak ilgili bir LNP kompozisyonunu seçtik. Ignite+ kullanarak düşük hacimlerde ve akış hızlarında kritik kalite özelliklerini (CQA'lar) belirliyoruz ve ardından akış hızını Blaze, ticari formülasyon sistemi ve modüler ticari formülasyon skid’i kullanarak 800 mL/dakika'ya kadar kademeli olarak artırıyoruz. Sistemler ve karıştırıcılar arasında ortak fizikokimyasal testler ve in vitro hücre hatları ve in vivo hayvan modellerinde biyolojik aktivite testleri kullanarak CQA'lar arasında eşdeğerlik sağladığımızı gösteriyoruz.
















